سلول الکترولیتی
سلول الکترولیتی از چه اجزائی تشکیل شده است؟
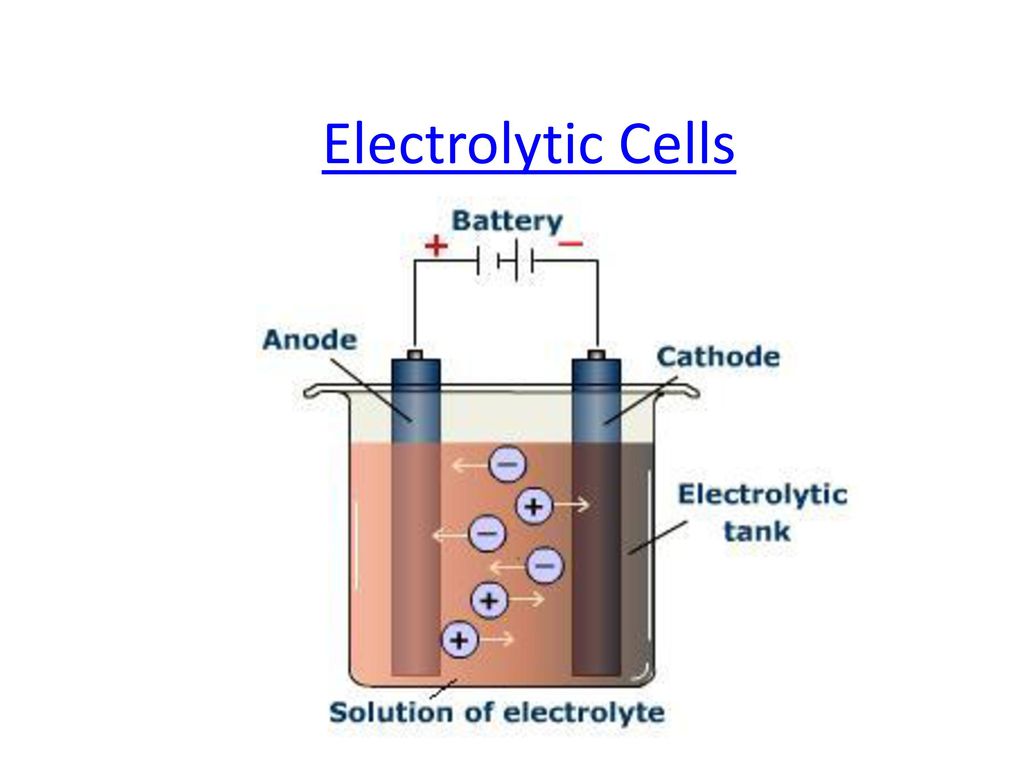
اجزاء یک سلول الکتروشیمیایی شامل یک الکترولیت و دو الکترود کاتد و آند است. الکترولیت معمولاً محلول آبی یا حلال دیگری است که یونها در آن حل می شوند. نمک های مذاب مانند کلرید سدیم نیز می توانند به عنوان الکترولیت استفاده شوند. هنگامی که الکترودها تحت یک ولتاژ خارجی قرار می گیرند یون های موجود در الکترولیت جذب الکترود با بار مخالف می شوند ، جایی که واکنش های انتقال بار (فارادایک یا ردوکس) اتفاق می افتد و انرژی الکتریکی را به انرژی شیمیایی تبدیل می شود. این سلول در فرآیندی موسوم به الکترولیز برای تجزیه ترکیبات شیمیایی مورد استفاده قرار می گیرد و فرآیندآبکاری نیز با استفاده از این سلول ها انجام می شود.
از تفاوت های سلول های الکترولیتی و سلول گالوانی که در پست بعدی توضیح خواهم داد این است در گالوانی از انرژی حاصل از واکنش خودبهخودی، انرژی الکتریکی بدست می آید ولی در سلول الکترولیتی، انرژی الکتریکی به انرژی شیمیایی تبدیل خواهد شد.
سلول الکترولیتی از دو نیم سلول اکسایش و کاهش تشکیل شده است. جریان پیوسته الکترون از آند به کاتد برقرار می کنیم. در محل آند، اکسایش صورت می گیرد و در محل کاتد کاهش.
سلول الکترولیتی روی و مس:

Oxidation: Zn(s) ----> Zn2+ + 2e- Oxidation
Reduction: 2 Cu+ (aq) + 2e- ----> 2 Cu(s) Reduction
دو طرفه معادله را با هم جمع می کنیم:
The balanced, net ionic equation for the reaction
Zn(s) + 2 Cu+ (aq) + 2e- -----> Zn2+ + 2 Cu(s) +2e
جهت شبیه سازی سلول الکترولیتی کلیک نمایید.
توضیحات نرم افزار شبیه سازی سلولهای الکترولیتی


